點擊關注不迷路 ↑ ↑
普及科學知識,傳播科學精神

B型肝炎病毒(HBV)是世界範圍內肝硬化和肝細胞癌的主要原因。目前,估計有超過20億人感染過B肝病毒,其中2.96億人(約占人口的3.7%)患有慢性B肝感染。慢性HBV感染每年導致全球約82萬人死於肝硬化和肝細胞癌併發症,儘管有有效的疫苗,每年仍有約150萬例新發感染。世界衛生組織制定了到2030年消除HBV的目標,即與2015年相比,HBV相關死亡率降低65%,發病率降低90%。
目前臨床中有很多關於HBV的療法進展,有望實現慢B肝功能性治癒(B肝表面抗原[HBsAg]消失)和完全治癒(清除共價閉合環狀DNA[cccDNA]和整合HBV DNA)。
近期,美國國立衛生研究院(NIH)國家糖尿病、消化和腎臟疾病研究所Marc G. Ghany教授等人的一篇綜述發表於消化領域權威期刊、美國胃腸病學會(AGA)會刊Gastroenterology,該綜述涵蓋了當前慢性HBV感染的最佳管理實踐和HBV感染的新興療法及其治癒前景。讓我們一起來看一看。

一、HBV感染治療目標
慢B肝治療的主要目標是預防肝硬化、肝細胞癌的發展和降低肝臟相關死亡率。不過,從感染到發生這些終點事件,病情發展通常需要經過幾十年。因此,評估慢性HBV感染治療方法的研究依賴於替代終點,包括HBV DNA水平低於可檢測下限、谷丙轉氨酶(ALT)正常化、B肝病毒e抗原(HBeAg)消失、HBsAg消失和組織學改善。
二、B肝當前治療選擇
肝臟學會指南推薦了兩種治療策略,一種是使用聚乙二醇干擾素α-2a進行48周療程治療,另一種是使用推薦的核苷(酸)類似物進行長期治療。其中核苷(酸)類似物包括拉米夫定、替比夫定、阿德福韋、恩替卡韋(ETV)、富馬酸替諾福韋二吡呋酯(TDF)和替諾福韋艾拉酚胺(TAF)。
1. 聚乙二醇干擾素α-2a
聚乙二醇干擾素α-2a具有抗病毒和免疫調節特性。HBeAg陽性患者使用該類藥物後,其HBeAg消失率相對較高(>30%),並有可能在相對較短的時間內清除HBsAg(HBeAg陽性患者HBsAg清除率為2%~7%,HBeAg陰性患者HBsAg清除率為4%),尤其是在HBV基因型A和B的患者中。此外,HBeAg消失和HBsAg消失是持久的。
不過該類藥物也存在一些缺點,包括需要皮下注射給藥,以及伴隨大量的不良事件發生。此外,由於肝臟失代償風險,聚乙二醇干擾素禁用於失代償性肝硬化和代償性肝硬化伴臨床顯著的門靜脈高壓症患者。
2. 核苷(酸)類似物
與聚乙二醇干擾素相比,核苷(酸)類似物口服給藥,耐受性好,是更有效的病毒複製抑制劑,但由於其不能直接抑制cccDNA的轉錄活性,因此在停藥後病毒複製復發很常見。
三、B肝當前治療的局限性
目前的療法不能治癒B肝感染,也不能消除肝細胞癌風險。這是由於這些療法對cccDNA和整合HBV DNA的影響有限。此外,目前的治療並不能恢復慢性HBV感染的免疫功能紊亂。因此,迫切需要能夠實現高HBsAg消失率的短期治療方案。
四、B肝新型療法
目前有很多治療慢性HBV感染的在研創新療法,包括阻斷病毒產生、恢復或增強免疫應答的創新療法。隨著新療法的發展,臨床上將需要一些新型標誌物來監測病毒學和免疫學應答,如HBV RNA,B型肝炎核心相關抗原(HBcAg)等。
1. 直接抗病毒藥物
1) 病毒進入抑制劑(靶向病毒進入的藥物)
靶向病毒進入的前提是阻斷新一輪肝細胞感染,從而防止cccDNA形成並減少cccDNA庫。Bulevirtide(既往稱為Myrcludex B)和Hepalatide均為牛磺膽酸鈉共轉運多肽受體阻滯劑,可阻止病毒進入。
與靶向受體不同,目前臨床中正在開發幾種單克隆/多克隆抗體製劑,其結合前S1的N末端區域,即病毒與牛磺膽酸鈉共轉運多肽受體相互作用的位點。除了阻斷病毒進入,單克隆抗體可以降低病毒血症和亞病毒顆粒水平,並可能通過刺激T細胞交叉呈現病毒抗原導致HBsAg消失。
GC1102是一種重組B型肝炎免疫球蛋白,目前正處於2期臨床試驗。VIR-3434是一種新型單克隆抗體,正在病毒抑制患者中進行1期研究;初步結果顯示,HBsAg水平呈劑量依賴性快速下降,無明顯不良事件發生。
2) 靶向病毒轉錄物的藥物
抑制病毒產生的另一種方法是通過RNA干擾(RNAi)和反義寡核苷酸(ASOs)靶向編碼信使RNA(mRNAs)的蛋白質。這種方法的治療優勢是單個小干擾RNA(siRNA)/ASO可以沉默多個病毒轉錄物。siRNA可以作為誘導療法在有限的療程內給藥以降低HBsAg水平。
兩種反義分子,bepirovirsen和IONIS-HBVLRx,目前正在接受核苷(酸)類似物治療的患者中進行2a期試驗。
3) 靶向核心蛋白的藥物
HBV核心蛋白在病毒生命周期和宿主免疫應答中具有多種調節作用,其主要作用是作為病毒核衣殼的結構蛋白,而核衣殼是病毒基因組的逆轉錄和複製位點。該核心蛋白還調節HBV基因組的亞細胞運輸和釋放、RNA代謝、cccDNA轉錄,並抑制宿主先天免疫應答。
核心蛋白變構調節劑(CpAMs)具有較強的病毒複製抑制作用。目前至少有12種CpAMs處於藥物開發的不同階段。CpAMs在抑制所有HBV基因型的HBV複製方面非常有效,不過該類藥物必須與一種或多種不同類型的抗病毒藥物聯合應用。CpAMs與核苷(酸)類似物聯合應用時,會帶來更快和更顯著的病毒複製抑制。
4) 靶向B型肝炎病毒聚合酶的藥物
靶向HBV聚合酶逆轉錄酶功能的藥物是治療慢性HBV感染廣泛使用的藥物。ATI-2173是一種B肝病毒聚合酶抑制劑。在1期研究中,28天給藥導致HBV DNA平均減少2.8 log10 IU/mL,無任何嚴重不良事件。預計在短暫的給藥間隔內,HBsAg水平沒有變化。該藥的2期研究正在進行中。
其他靶向HBV聚合酶如pradefovir、HS-10234,分別源自阿德福韋和替諾福韋,旨在提高抗病毒效力並降低代謝物毒性。初步數據表明,其有效性與TDF相似。靶向HBV聚合酶RNase H功能的藥物正在臨床前開發中。
5) 靶向HBsAg釋放的藥物
HBsAg在慢性HBV感染中以亞病毒顆粒的形式大量循環。核酸聚合物(NAP)是一種短的合成寡核苷酸,能夠與HBV亞病毒顆粒相互作用並阻斷分泌。
阻斷HBsAg分泌的類似方法包括S-抗原轉運抑制寡核苷酸聚合物(STOPS)。與NAP相似,STOPS是一種單鏈寡核苷酸,可以隔離HBsAg產生所需的細胞蛋白。體外研究表明,STOPS比NAP具有更大的效力。
6) 靶向cccDNA的藥物
消除肝細胞核內的cccDNA是治癒慢性HBV感染的關鍵。有幾種消除或沉默cccDNA的方法正在臨床前開發中。
基因編輯技術,如鋅指核酸酶、轉錄激活因子樣效應核酸酶和CRISPR/Cas-9蛋白,通過在DNA中引入靶向雙鏈斷裂,然後通過同源修復在裂解位點產生突變來滅活cccDNA。該類技術目前正在評估中。在一項對HBV感染細胞系進行的研究中,CRISPR/Cas9技術成功地消除了90%的HBV cccDNA。
此外,靶向HBV X蛋白(HBX)可能是沉默cccDNA的可行方法。Pevonedistat和dicoumarol顯示可降低HBX表達。
通過上調APOBEC3A/B可導致cccDNA降解,該療法也可為靶向cccDNA的前景應用。
2. 間接抗病毒藥物
目前與治療相關的一個問題是,是否可以通過純抗病毒方法實現治癒,或者是否有必要添加免疫調節劑。目前的免疫學方法均針對先天性和適應性免疫系統,以廣泛增強細胞防禦並促進HBV適應性免疫應答。
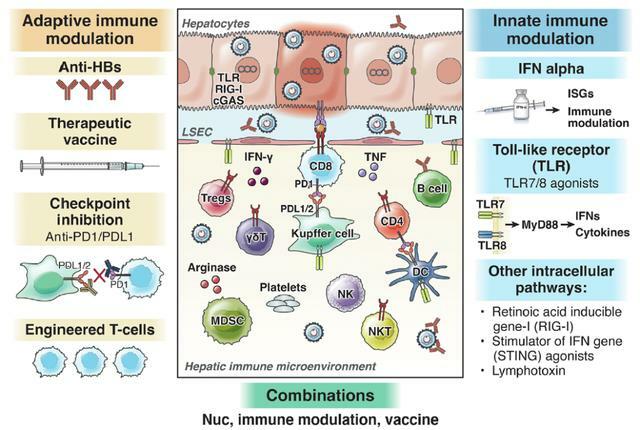
1) 先天免疫激動劑
Toll樣受體(TLRs)在許多細胞亞群中表達,並作為病毒和細菌病原體相關分子模式的傳感器在宿主防禦中發揮重要作用。幾種口服TLR-7/8激動劑正在進行臨床試驗,包括GS-9620、RO7020531、RG7795、JNJ-4964和GS-9688。
2) 刺激和恢復適應性免疫的藥物
目前臨床上已經探索了幾種策略來重新激活對HBV的弱適應性免疫應答,其中一個關鍵考慮因素是安全地誘導治療應答,而不會引起嚴重的肝細胞損傷和臨床失代償。
- 免疫檢查點抑制劑
最近的一項2期研究評估了PD-1單克隆抗體envafolimab(ASC22)用於既往接受核苷(酸)類似物治療的患者的效果,結果觀察到HBsAg降低可達1.2 log10 IU/mL。
另一種靶向PD-1途徑的方法是通過核糖核酸酶H(RNAseH)途徑降解PD-1配體mRNA。
儘管免疫檢查點抑制劑可能有效,不過對其安全性和不可預測反應還需進行更大規模的研究。
- 基因編輯T細胞
B肝治療研究的新思路,如過繼轉移設計基因編輯HBV特異性T細胞(包括嵌合抗原受體T細胞[CAR-T]和T細胞受體T細胞[TCR-T]等),該方法可以更新替代體內耗竭的T細胞,產生功能性T細胞,以消除HBV感染的肝細胞。
3) 新型治療性疫苗
治療性疫苗接種的前提是打破免疫耐受,增強HBV特異性T細胞應答,以介導功能性治癒(HBsAg消失)。不過先前使用多種抗原(前S1/S2)、肽基T細胞疫苗、帶有新型佐劑的DNA疫苗等的嘗試均未成功。更新的疫苗方法採用獨特的策略來提高疫苗效力,包括納入多種抗原以擴大T細胞應答;改進遞送系統;採用新型佐劑;聯合檢查點抑制劑應用;使用病毒載體等。不過這些策略還需進一步研究。
結論
慢性HBV感染有終生發展為肝硬化和肝癌的風險。存在肝硬化和肝癌風險的人應接受抗病毒治療。雖然目前的治療與改善臨床結果相關,但由於缺乏對cccDNA和整合HBV DNA的作用,其療效不佳。此外,在沒有HBsAg消失的情況下停止治療通常會導致大多數患者疾病復發,因此必須進行長期治療。
鑑於全球疾病負擔,迫切需要更有效的治療。目前有多種治療慢性HBV感染的新療法。而實現功能性治癒可能需要多種藥物的組合,包括抗病毒藥物、減少病毒抗原負荷的藥物和增強免疫應答的免疫調節劑等。完全治癒需要完善基因編輯療法。
參考資料
[1] Yardeni D, et al., (2022). Current Best Practice in Hepatitis B Management and Understanding Long-term Prospects for Cure. Gastroenterology, doi: 10.1053/j.gastro.2022.10.008.
免責聲明:藥明康德內容團隊專注介紹全球生物醫藥健康研究進展。本文僅作信息交流之目的,文中觀點不代表藥明康德立場,亦不代表藥明康德支持或反對文中觀點。本文也不是治療方案推薦。如需獲得治療方案指導,請前往正規醫院就診。
版權說明:本文來自藥明康德內容團隊,歡迎個人轉發至朋友圈,謝絕媒體或機構未經授權以任何形式轉載至其他平台。